

Verifarma Medical Devices to kompleksowe rozwiązanie, pozwalające producentom wyrobów medycznych na zarządzanie etykietami, zgłoszeniami i wymogami jakościowymi w odniesieniu do europejskich przepisów dotyczących wyrobów medycznych (MDR) i wyrobów medycznych do diagnostyki in vitro (IVDR).
Wszechstronny zestaw rozwiązań Verifarmy pozwala producentom wyrobów medycznych na zarządzanie procesem etykietowania, zgłaszania i wymogów jakościowych, w zgodności z nadchodzącymi przepisami UE dotyczących wyrobów medycznych (MDR) i wyrobów medycznych do diagnostyki in vitro (IVDR).
Nowe przepisy UE dotyczące wyrobów medycznych
(przyjęte 5 kwietnia 2017 i opublikowane 5 marca 2017)
- Dyrektywa 90/385/CEE dotycząca wyrobów medycznych aktywnego osadzania
- Dyrektywa 93/42/CEE dotycząca wyrobów medycznych
- Dyrektywa 98/79/CE dotycząca wyrobów medycznych używanych do diagnozy in vitro
Główne zmiany nowych przepisów:
- Włączenie w zakres niektórych urządzeń estetycznych
- Minimalne wymagania dotyczące utylizacji produktów jednokrotnego użytku
- Ostrzejsza kontrola urządzeń wysokiego ryzyka przez MDCG przed zwolnieniem na rynek
- Dodatkowe zasady badań i testów klinicznych
- Zwiększone znaczenie i nadzór organów kontrolnych
- Założenie rozległej europejskiej bazy danych wyrobów medycznych (EUDAMED). Udostępnienie wielu informacji publicznie
- Wprowadzenie systemu UDI
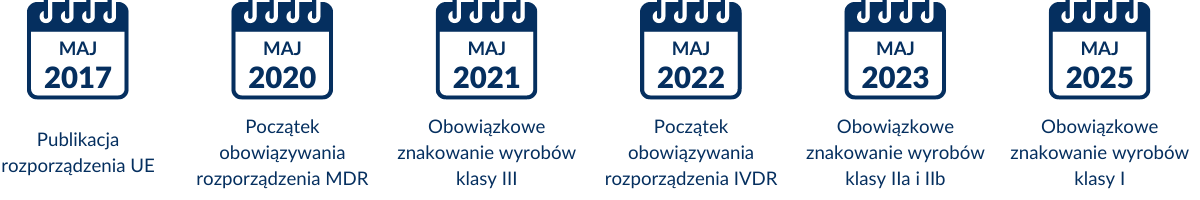
Główne terminy:

Zapytaj o produkt

Verifarma MD – UDI
Rozwiązanie do etykietowania wyrobów medycznych na poziomie przedsiębiorstwa. Rozwiązuje problem generowania i drukowania informacji (UDI) na etykiecie/opakowaniu wyrobu medycznego.
Verifarma MD – Zarządzanie UDI
Rozwiązanie do etykietowania urządzeń medycznych na poziomie przedsiębiorstwa. Rozwiązuje problem generowania i drukowania informacji (UDI) na etykiecie/opakowaniu urządzenia.
- Przydzielanie numerów identyfikacyjnych dla wszystkich wyrobów oraz poziomów pakowania, w tym zestawów i produktów złożonych
- Generowanie numerów seryjnych / numerów partii
- Zarządzanie master data struktury UDI: definiowanie nośników danych i ich zawartości
- Wsparcie przy uzyskaniu członkostwa organów wydających kody firmowe (np. GS1, HIBCC)
- Zarządzanie UDI
- Nadawanie nowych UDI-DI
- Automatyczne połączenie z drukarkami, skanerami i liniami produkcyjnymi.
- Przechowywanie i zarządzanie danymi
VERIFARMA MD - EUDAMED
Rejestracja oraz raportowanie wymaganych informacji do odpowiedzialnych organów. Zgłaszanie wymaganych informacji (UDI, dane, dokumenty) do Eudamed oraz partnerów biznesowych.
- Centralne zarządzanie danymi
- Raportowanie danych do Eudamed
- Automatyczne interfejsy z partnerami biznesowymi w celu wymiany informacji
- Integracja z systemem ERP, czy WAMAS
- Długoterminowe przechowywanie oraz administracja danych
- Aktualizowanie danych


VERIFARMA QUALITY
Moduł zarządzania jakością.
- Wprowadzenie system zapewniającego jakość danych
- Implementacja procesu kontroli zmian dla nowych i modyfikowanych danych
- Zarządzanie Standardowymi Procedurami Operacyjnymi
- Śledzenie programów/wydarzeń
- Zarządzanie audytem wewnętrznym i zewnętrznym
- Zarządzanie ryzykiem
- Lokalizowanie potencjalnych braków w odniesieniu do ustalonych wymagań
- Zarządzanie reklamacjami jakościowymi
- Kwalifikacja partnerów (GMP)



